Símbolo del hidrógeno. Autor: desconocido.
El hidrógeno es el elemento químico representado por el símbolo H y con el número atómico «1». Con una masa atómica de 1,00794(7) u, el hidrógeno es el elemento químico más ligero y, también, el más abundante, constituyendo aproximadamente el 73,9% de la materia visible del universo.
En su ciclo principal, las estrellas están compuestas por hidrógeno en estado de plasma, pero en la Tierra el hidrógeno elemental es muy escaso, por lo que tiene que ser producido industrialmente a partir de hidrocarburos como, por ejemplo, el metano. La mayor parte del hidrógeno elemental se obtiene «in situ«, es decir, en el lugar y en el momento en el que se necesita. El hidrógeno puede obtenerse a partir del agua por un proceso de electrólisis, pero resulta un método mucho más caro que la obtención a partir del gas natural.
Sus principales aplicaciones industriales son el refinado de combustibles fósiles (por ejemplo, el hidrocracking) y la producción de amoníaco (usado principalmente para fertilizantes).
El hidrógeno puede formar compuestos con la mayoría de los elementos y está presente en el agua y en la mayoría de los compuestos orgánicos. Desempeña un papel particularmente importante en la química ácido-base, en la que muchas reacciones conllevan el intercambio de protones entre moléculas solubles. Puesto que es el único átomo neutro para el cual la ecuación de Schrödinger puede ser resuelta analíticamente, el estudio de la energía y del enlace del átomo de hidrógeno ha sido fundamental para el desarrollo de la mecánica cuántica.
Isótopos:
El hidrógeno posee tres isótopos naturales que se denotan como 1H, 2H y 3H. Otros isótopos altamente inestables (del 4H al 7H) han sido sintetizados en laboratorio, pero nunca observados en la naturaleza.
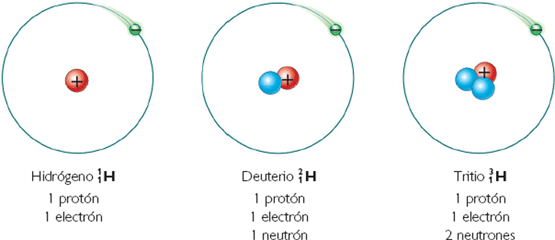
Los tres isótopos estables del hidrógeno: protio, deuterio y tritio. Autor: desconocido.
- 1H –> Conocido como protio, es el isótopo más común del hidrógeno con una abundancia de más del 99,98%. Debido a que el núcleo de este isótopo está formado por un solo protón (no tiene ningún neutrón) se le ha bautizado como protio, nombre que a pesar de ser muy descriptivo es poco usado.
- 2H –> Otro isótopo estable del hidrógeno es el deuterio; su núcleo contiene un protón y un neutrón. El deuterio representa el 0,0026% o el 0,0184% (según sea en fracción molar o fracción atómica) del hidrógeno presente en la Tierra, encontrándose las menores concentraciones en el hidrógeno gaseoso, y las mayores (0,015% o 150 ppm) en aguas oceánicas. El deuterio no es radiactivo, y no representa un riesgo significativo de toxicidad. El agua enriquecida en moléculas que incluyen deuterio en lugar de hidrógeno 1H (protio) se denomina agua pesada.
El deuterio y sus compuestos se emplean en marcado no radiactivo en experimentos y también en disolventes usados en espectroscopia 1H – RMN. El agua pesada se utiliza como moderador de neutrones y refrigerante en reactores nucleares. El deuterio es también un potencial combustible para la fusión nuclear con fines comerciales.

Núcleo de deuterio y electrón orbitando en torno a él. Autor: Xaquito.
- 3H –> Se conoce como tritio y contiene un protón y dos neutrones en su núcleo; es radiactivo, desintegrándose en 32He+ a través de una emisión beta. Posee un periodo de semidesintegración de 12,33 años.
Pequeñas cantidades de tritio se encuentran en la naturaleza por efecto de la interacción de los rayos cósmicos con los gases atmosféricos. También ha sido liberado tritio por la realización de pruebas de armamento nuclear. El tritio se usa en reacciones de fusión nuclear, como trazador en Geoquímica Isotópica, y en dispositivos luminosos autoalimentados. Antes era común emplear el tritio como radiomarcador en experimentos químicos y biológicos, pero actualmente se utiliza menos.
El hidrógeno es el único elemento que posee diferentes nombres comunes para cada uno de sus isótopos naturales. Durante los inicios de los estudios sobre la radiactividad, a algunos isótopos radiactivos pesados les fueron asignados nombres, pero ninguno de ellos se sigue usando. Los símbolos D y T (en lugar de 2H y 3H) se usan a veces para referirse al deuterio y al tritio, pero el símbolo P corresponde al fósforo y, por tanto, no puede usarse para representar al protio. La IUPAC declara que aunque el uso de estos símbolos sea común, no es lo aconsejado.
Moléculas:
En condiciones normales de presión y temperatura, el hidrógeno forma un gas diatómico incoloro, inodoro, insípido, no metálico y altamente inflamable cuya fórmula es H2. Existen dos tipos distintos de moléculas diatómicas de hidrógeno que difieren en la relación entre los espines de sus núcleos:
- Orto-hidrógeno: los espines de los dos protones se encuentran paralelos y conforman un estado triplete (tres posibles valores de espín).
- Para-hidrógeno: los espines de los dos protones se encuentran antiparalelos y conforman un estado singlete (un posible valor de espín).
En condiciones normales de presión y temperatura el hidrógeno gaseoso contiene aproximadamente un 25% de la forma para- y un 75% de la forma orto-, también conocida como «forma normal». La relación del equilibrio entre orto-hidrógeno y para-hidrógeno depende de la temperatura, pero puesto que la forma orto- es un estado excitado, y por tanto posee una energía superior, es inestable y no puede ser purificada. A temperaturas muy bajas, el estado de equilibrio está compuesto casi exclusivamente por la forma para-. Las propiedades físicas del para-hidrógeno puro difieren ligeramente de las de la forma normal orto-. La distinción entre formas orto-/para- también se presenta en otras moléculas o grupos funcionales que contienen hidrógeno, como el agua.
La interconversión no catalizada entre el para-hidrógeno y el orto-hidrógeno se incrementa al aumentar la temperatura; por esta razón, el H2 condensado rápidamente contiene grandes cantidades de la forma orto- que pasa a la forma para- lentamente. La relación orto-/para- en el H2 condensado es algo importante a tener en cuenta para la preparación y el almacenamiento del hidrógeno líquido: la conversión de la forma orto- a la forma para- es exotérmica y produce el calor suficiente para evaporar el hidrógeno líquido, provocando la pérdida del material licuado. Catalizadores para la interconversión orto-/para-, tales como compuestos de hierro, son usados en procesos de refrigeración con hidrógeno.
Una forma molecular llamada «hidrógeno molecular protonado«, H3+, se encuentra en el medio interestelar, donde se genera por la ionización del hidrógeno molecular provocada por los rayos cósmicos. También se ha observado en las capas superiores de la atmósfera de Júpiter. Esta molécula es relativamente estable en el medio del espacio exterior debido a las bajas temperaturas y a la bajísima densidad. El H3+ es uno de los iones más abundantes del universo y juega un papel notable en la química del medio interestelar.
En los compuestos iónicos, el hidrógeno puede adquirir carga positiva (convirtiéndose en un catión compuesto únicamente por el protón) o negativa (convirtiéndose en un anión conocido como hidruro).
Curiosidades:
Si bien se suele catalogar al hidrógeno como no metal, a bajas temperaturas y altas presiones puede comportarse como metal. En marzo de 1996, un grupo de científicos del Laboratorio Nacional Lawrence Livermore informó de que habían producido casualmente, durante un microsegundo y a temperaturas de miles de grados Kelvin y presiones de más de un millón de atmósferas (>100 GPa), el primer hidrógeno metálico identificable.
****************************************************************************************************************************
Figuras:
La siguiente figura tiene una licencia Creative Commons Attribution 3.0 Unported o posterior. Para la publicación de la misma en otros medios no es necesario solicitar permiso al autor (indicado, en el texto, debajo de la figura), pero debe ser referenciada correctamente, mostrando la página web del mismo o, en su defecto, la página que aquí abajo se indica.
–Colaboradores de Wikipedia (2009). «Atomo hidrogeno.gif». Wikipedia, la enciclopedia libre. [link]
Es probable que las siguientes figuras tengan copyright. Para la publicación de las mismas en otros medios se debe solicitar permiso al autor correspondiente (indicado, en el texto, debajo de cada figura) y referenciarlas correctamente, mostrando su página web o, en su defecto, la página correspondiente que aquí abajo se indica.
–Anne Marie Helmenstine, Ph.D., (2013). «Hydrogen. Hydrogen Facts and Properties». About.com. Education. Chemistry. [link]
–Equipo de Prensa (2010). «Isótopos y ejemplos». Blog de Química. [link]
Referencias:
–Colaboradores de Wikipedia (2009). “Hidrógeno”. Wikipedia, la enciclopedia libre. [link]


